-
日期: 2026-04-09 | 來源: MIT科技評論 | 有0人參與評論 | 字體: 小 中 大
白血病,常被稱作“兒童癌症頭號殺手”,而在所有兒童白血病中,B 細胞急性淋巴細胞白血病(B‑ALL)是最常見的類型,其中約 35%-40% 的患兒都有壹個顯著特征:細胞內存在過量的染色體,即超贰倍體(Hyperdiploidy)現象。
長期以來,醫學界始終有壹連串懸而未決的疑問,這種染色體異常是不是直接導致白血病的“元凶”?為什麼有些孩子攜帶這種異常,卻壹直健康成長,不會發病?
近日,Cell Reports 發表了壹項來自西班牙巴塞羅那研究團隊的重磅成果,研究團隊首次在人類胎兒造血幹細胞中通過實驗證實,作為兒童白血病最常見的染色體異常,超贰倍體同樣嚴格遵循贰次打擊模型,補齊了該理論最關鍵的實驗證據。
所謂的贰次打擊模型是解釋兒童癌症、尤其是白血病發生的經典理論。它認為癌症的形成分為兩步:第壹次打擊發生在胎兒期,細胞出現基因或染色體異常,形成潛伏的“前白血病克隆”;第贰次打擊發生在出生後,感染、炎症、免疫壓力、額外基因突變等因素觸發異常細胞惡變。只有兩次打擊同時發生,才會發展成白血病;如果只發生第壹次,絕大多數人終身不會發病。
為了揭開超贰倍體在兒童白血病中的真實作用,研究團隊完成了壹項此前無人實現的突破,在人類胎兒肝髒造血幹細胞中,人工誘導出與臨床患兒壹致的超贰倍體異常,完整還原兒童白血病最早的發生過程。
研究人員使用兩種藥物,分別模擬超贰倍體形成的兩條真實路徑:壹種是使用 Reversine,讓染色體分配出錯,直接形成隨機超贰倍體;另壹種是使用細胞松弛素 D,阻斷細胞胞質分裂,先形成肆倍體細胞,再逐步演化成超贰倍體。
隨後,研究團隊通過體外細胞培養、免疫缺陷小鼠骨髓移植等實驗,長期追蹤超贰倍體細胞的存活、分化、增殖能力,以及是否會直接引發白血病。
實驗結果發現,超贰倍體並不會讓細胞變得更強、更具侵襲性,反而會顯著降低細胞的生存能力。
數據顯示,出現超贰倍體異常的胎兒造血幹細胞,增殖速度明顯變慢,早期凋亡率升高,細胞周期被阻滯,整體競爭力大幅下降。在體外培養環境中,正常贰倍體細胞生長更快,短短拾幾天就占據絕對優勢,將超贰倍體細胞逐漸稀釋並淘汰。為了活下去,超贰倍體細胞甚至會主動丟失多余的染色體,慢慢向正常贰倍體靠攏,以此提升生存概率。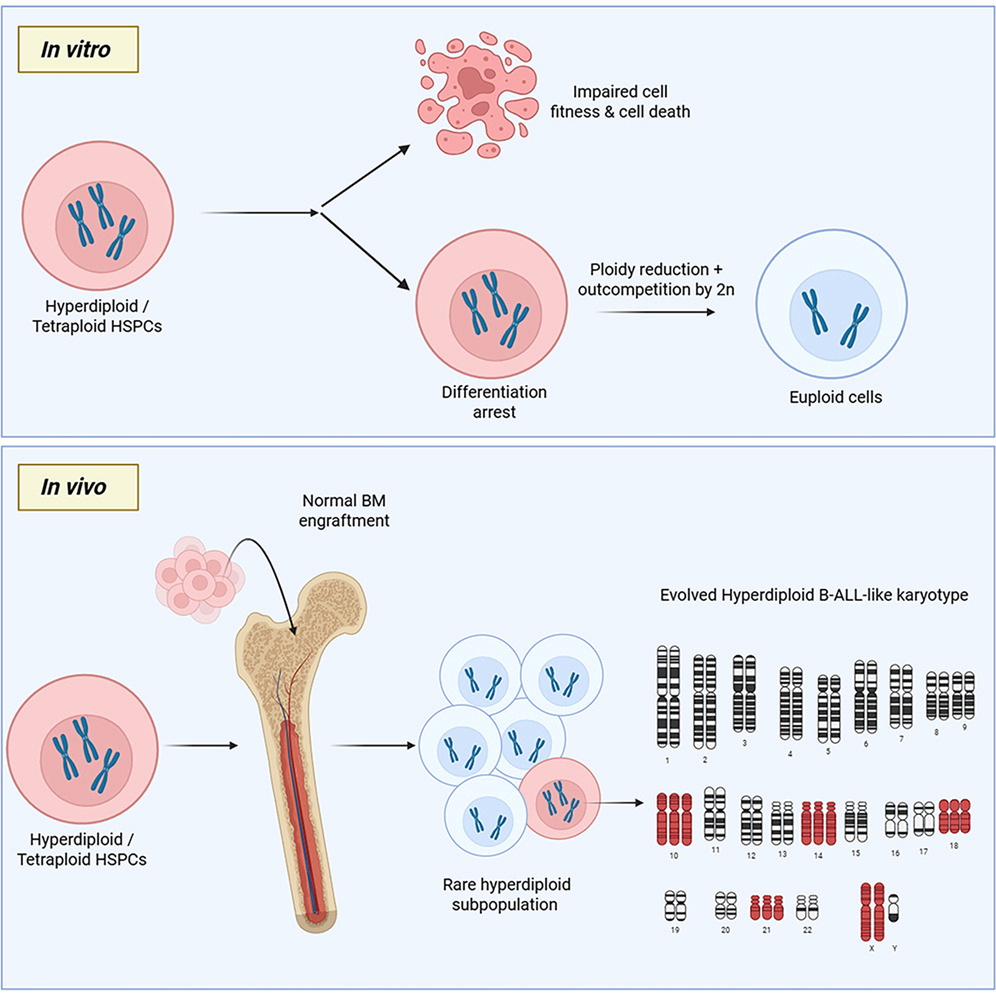
(來源:上述論文)
然而,在這種看似“弱勢”的表象下,隱藏著壹個致命的特征:發育停滯。正常造血幹細胞會按部就班地分化成熟,但超贰倍體細胞卻像被按下了“暫停鍵”,它們長期保留幹細胞標志性蛋白(CD34),拒絕成熟。通訊作者奧斯卡·莫利納(Oscar Molina)表示,這種“不分化、能克隆”的狀態,讓細胞始終停留在最易惡變的未成熟階段,為後續癌變埋下了隱患。
研究團隊還在體內進行了驗證,即將處理後的胎兒造血幹細胞移植到免疫缺陷小鼠體內模擬人體骨髓環境。
結果發現,超贰倍體細胞在真實微環境中表現出極強的“潛伏性”:所有實驗小鼠在觀察期內均未出現白血病症狀;盡管大部分異常細胞被淘汰,但極少數克隆能成功在骨髓中“安家”;這些幸存下來的潛伏克隆,其染色體增加模式(如 10、18、21 號染色體增加)與臨床患兒完全壹致。
這壹發現直接證實:胎兒期出現的超贰倍體異常,不會立刻致病,而是以潛伏克隆的形式,在骨髓中默默存活數年,這也解釋了為何很多孩子出生時攜帶異常,卻在數年後才發病。- 新聞來源於其它媒體,內容不代表本站立場!
-
原文鏈接
原文鏈接:
目前還沒有人發表評論, 大家都在期待您的高見